Περίληψη
Έχουν περάσει σαράντα χρόνια αφότου σχεδιάστηκε η τεχνική για την μέτρηση και την παρακολούθηση των βασικών αιμοδυναμικών παραμέτρων σε ανθρώπους με την μέθοδο της καρδιογραφίας αντίστασης που είναι επίσης γνωστή ως πληθυσμογραφία αντιστάσεων του θώρακα ή ηλεκτρική βιοαντίσταση του θώρακα. Με την μέθοδο αυτή υπολογίζουμε τον όγκο παλμού και την καρδιακή παροχή, μπορούμε να εκτιμήσουμε το προφορτίο μέσω της εκτίμησης της περιεκτικότητας του θώρακα σε υγρά, το μεταφορτίο με την μέτρηση των συστηματικών αγγειακών αντιστάσεων και της συσταλτικότητας – φορτίου, με την μέτρηση του δείκτη επιτάχυνσης και του δείκτη ταχύτητας. Επιπροσθέτως υπολογίζονται η προσυστολική ή προεξωθητική περίοδος, ο χρόνος συστολής και ο χρόνος εξώθησης της αριστεράς κοιλίας, η χρονική αναλογία της συστολικής περιόδου και ο καρδιακός ρυθμός. Η επιτευχθείσα πρόοδος στα ψηφιακά ηλεκτρονικά συστήματα σημάτων και η ανάπτυξη αλγορίθμων βελτίωσαν σημαντικά την ποιότητα και την αξιοπιστία των προσλαμβανόμενων τιμών.
Η ακρίβεια και η επαναληψιμότητα των αποτελεσμάτων επιβεβαιώθηκαν από μελέτες που συγκρίνανε τα ευρήματα της μεθόδου με τα αντίστοιχα μετά από υπερηχογραφικές ή επεμβατικές μεθόδους. Η διαγνωστική μέθοδος εφαρμόστηκε με απόλυτη επιτυχία σε μονάδες εντατικής θεραπείας, σε χειρουργικές επεμβάσεις και κατά την διάρκεια της αιμοκάθαρσης. Επίσης εφαρμόστηκε επιτυχώς σαν επαναλαμβανόμενη μέθοδος εκτίμησης των αιμοδυναμικών παραμέτρων για την αξιολόγηση της θεραπευτικής αγωγής σε υπερτασικούς ασθενείς και σε πάσχοντες από καρδιακή ανεπάρκεια, όπως και σε καρδιοπαθείς εγκυμονούσες. Προτείνεται δε σήμερα η μέθοδος σαν εξέταση αρχικής εκτίμησης τόσο ασθενών ευρισκόμενων σε σοβαρή κατάσταση στα τμήματα πρώτων βοηθειών όσο και σε κάθε ασθενή με δύσπνοια, υπέρταση ή υπόταση, ή σε κάθε ασθενή που πάσχει από πνευμονική υπέρταση ή προγραμματίζεται για κολποκοιλιακή ή αμφικοιλιακή βηματοδότηση. Η μέθοδος αποδεικνύεται πολύτιμο διαγνωστικό εργαλείο χωρίς κλινικά προβλήματα ή τεχνικές δυσκολίες, χωρίς τους κινδύνους της επεμβατικής παρακολούθησης της πνευμονικής κυκλοφορίας και χωρίς τους μικρούς αλλά υπαρκτούς κινδύνους ή τους περιορισμούς από τις χρονοβόρες ημιεπεμβατικές υπερηχογραφικές δοκιμασίες. Οι περιορισμοί της μεθόδου είναι ελάχιστες, περιλαμβάνουν μόνο άτομα με ακραία ανθρωπομετρικά χαρακτηριστικά, πάσχοντες από επίμονες και σοβαρές αρρυθμίες και βηματοδοτημένους με αισθητήρα minute validation.
Η καρδιογραφία αντίστασης στην αρτηριακή υπέρταση
Η ICG χρησιμοποιείται στην διάγνωση και στην θεραπεία των υπερτασικών ασθενών. Παρόλο που η αρτηριακή υπέρταση καθορίζεται από τις αυξημένες τιμές αρτηριακής πίεσης αίματος, σχετίζεται επίσης με ανώμαλη καρδιακή παροχή, με τις αγγειακές αντιστάσεις και με την ενδοτικότητα των αρτηριών. Η αρτηριακή ενδοτικότητα (susceptibility) ορίζεται ως η σχέση του όγκου παλμού SV (stroke volume) προς την πίεση παλμού PP (pulse pressure) και εκφράζει την διαφορά μεταξύ της συστολικής και διαστολικής αρτηριακής πίεσης.
Η γνώση των αιμοδυναμικών παραμέτρων επί αρτηριακής υπέρτασης έχει μεγάλη σημασία στην αιτιολογική διάγνωση, στην ολοκληρωμένη αξιολόγηση της κυκλοφορίας του αίματος, στην εκτίμηση του βαθμού κινδύνου και στην κλινική αξιολόγηση της ακολουθούμενης θεραπείας. Η αρτηριακή υπέρταση δεν αποτελεί από μόνη της επαρκές κριτήριο αξιολόγησης όλου του κυκλοφοριακού συστήματος. Η μέση αρτηριακή πίεση (mean arterial pressure, MAP) είναι εξαρτώμενη από δυο άλλους αιμοδυναμικούς παραμέτρους, την καρδιακή παροχή (cardiac output, CO) και τις συστηματικές αγγειακές αντιστάσεις (systemic vascular resistance, SVR). Η αρτηριακή υπέρταση μπορεί να είναι αποτέλεσμα αυξημένης καρδιακής παροχής ή αυξημένων αγγειακών περιφερικών αντιστάσεων ή συναύξησης και των δυο αυτών παραμέτρων. Οι αιμοδυναμικές παρατηρήσεις με την ICG επιτρέπουν την αιτιολογική διαφορική διάγνωση αυτών των ασθενών, διακρίνοντας αυτούς που έχουν αυξημένη καρδιακή παροχή από αυτούς που έχουν αυξημένες αγγειακές αντιστάσεις ή αυτούς που παρουσιάζουν συνύπαρξη και των δυο αυτών μηχανισμών.
Στις μελέτες των Linb και Eisenberg όπου αξιολογήθηκε η αντιυπερτασική θεραπεία με την μέθοδο της ICG, η χρήση ενός β-αναστολέα, της προπρανολόλης, είχε ευνοϊκή αντιυπερτασική επίδραση σε ασθενείς με αυξημένη καρδιακή παροχή, ενώ ο αναστολέας ασβεστίου (διυδροπυριδίνη) νιφεδιπίνη ήταν αποτελεσματικός στην κάμψη της υπέρτασης των ασθενών με αυξημένες περιφερικές αγγειακές αντιστάσεις. Επίσης παρατήρησαν ότι με την πάροδο του χρόνου, καθώς οι ασθενείς είχαν όλο και μεγαλύτερη ηλικία, σημειώνεται σταδιακά μείωση της καρδιακής παροχής και αύξηση των περιφερικών αγγειακών αντιστάσεων. Επομένως, σε νέους ενήλικες συνήθως η υπέρταση σχετίζεται με αυξημένη καρδιακή παροχή ενώ σε πιο ηλικιωμένους συνδέεται με αύξηση των αγγειακών αντιστάσεων.
Η ICG μπορεί να χρησιμοποιηθεί με επιτυχία για την εκτίμηση του κινδύνου εμφάνισης επιπλοκών από την αρτηριακή υπέρταση. Η ερευνητική ομάδα του Galarza εξέτασε με την μέθοδο της ICG δυο ομάδες υπερτασικών ασθενών, εκ των οποίων η πρώτη είχε ιστορικό αγγειακού εγκεφαλικού επεισοδίου ενώ η δεύτερη ήταν ελεύθερη τέτοιου ιστορικού. Διαπίστωσαν ότι στην πρώτη ομάδα η καρδιακή παροχή ήταν πλέον μειωμένη και οι περιφερικές αγγειακές αντιστάσεις περισσότερο αυξημένες. Αυτές οι διαφορές ήταν παρούσες και εμμένουσες παρά την επίτευξη ταυτόσημου αντιυπερτασικού αποτελέσματος και παρά την χορήγηση ίδιας αντιυπερτασικής αγωγής.
Η μέθοδος της ICG χρησιμοποιήθηκε για την εκτίμηση της μη φαρμακευτικής αντιμετώπισης των ασθενών με καλοήθη αρτηριακή υπέρταση. Σε ασθενείς που τέθηκαν σε δίαιτα με χαμηλή περιεκτικότητα νατρίου, η καρδιογραφία αντίστασης έδειξε μείωση του όγκου παλμού, ελάττωση της διαστολικής αρτηριακής πίεσης, αύξηση της βασικής αντίστασης του θώρακα, ελάττωση της περιεκτικότητας σε υγρά του θώρακα (thoracic fluid content, TFC) και μείωση του όγκου των εξωκυττάριων υγρών. Οι μετρήσεις όλων των επιμέρους αιμοδυναμικών παραμέτρων είναι χρήσιμες στην επιλογή του είδους της αντιυπερτασικής θεραπείας, στην επιλογή της δόσης των φαρμάκων και στην εκτίμηση της αποτελεσματικότητας της θεραπείας. Μεγάλη σειρά δημοσιεύσεων ερευνητικών δεδομένων έχει δείξει ότι η αντιυπερτασική θεραπεία που εφαρμόζεται στηριζόμενη στα αιμοδυναμικά δεδομένα της ICG, επιφέρει βέλτιστο αποτέλεσμα στον έλεγχο της αρτηριακής πίεσης.
Οι Taler και συν. εξέτασαν 104 υπερτασικούς ασθενείς που παρουσίαζαν ανεπαρκή ρύθμιση της αρτηριακής πίεσης, ενώ ελάμβαναν δυο ή και περισσότερα φάρμακα. Οι ασθενείς αυτοί τυχαιοποιήθηκαν σε δυο ομάδες, εκ των οποίων η πρώτη έλαβε αντιυπερτασική αγωγή καθοδηγούμενη από τις αιμοδυναμικές παραμέτρους της καρδιογραφίας αντίστασης, ενώ η δεύτερη ακολούθησε την κλασσική εμπειρική θεραπεία. Ως κριτήριο επαρκούς ρύθμισης αναγνωρίστηκε η επίτευξη πίεσης κάτω από 140 και 90 mmHg συστολικής και διαστολικής πίεσης αντιστοίχως. Σύμφωνα με τα αποτελέσματά τους, η επίτευξη σωστής ρύθμισης ήταν 70% συχνότερη στην ομάδα που καθοδηγείτο από την καρδιογραφία αντίστασης. Σε αυτή την ομάδα παρατηρήθηκε μεγαλύτερη πτώση των αγγειακών αντιστάσεων, ενώ ταυτόχρονα χρησιμοποιήθηκε πιο έντονη διουρητική αγωγή, βασιζόμενη στα επίπεδα της περιεκτικότητας του θώρακα σε υγρό (TFC).
Σε ασθενείς με ανθεκτική αρτηριακή υπέρταση, δηλαδή σε ασθενείς όπου η συστολική πίεση εξακολουθεί να είναι πάνω από 140 mmHg ή η διαστολική πίεση πάνω από 90 mmHg παρά την λήψη αγωγής, οι Sharman και συν. εφάρμοσαν θεραπευτικό πρωτόκολλο με χορήγηση δυο φαρμάκων, καθοδηγούμενοι από τις αιμοδυναμικές υποδείξεις της καρδιογραφίας αντίστασης. Με τον τρόπο αυτό κατάφεραν νορμοτασική ρύθμιση στο 51,7 % των ανθεκτικών υπερτασικών, στους οποίους πριν δεν είχε γίνει διαγνωστική χρήση και θεραπευτική αξιοποίηση των ευρημάτων της καρδιογραφίας αντίστασης. Παρόμοια ευρήματα και παρεμφερή θεραπευτικά συμπεράσματα ανέφεραν οι Shramek και συν., οι οποίοι συμπέραναν ότι η χρήση της καρδιογραφίας αντίστασης βοηθάει στην βέλτιστη αντιυπερτασική αγωγή. Επίσης συμπέραναν ότι οι αποκλίσεις των τιμών των αιμοδυναμικών παραμέτρων από τις αναμενόμενες, είτε υποδεικνύουν τους ασθενείς που διέκοψαν πρώιμα την θεραπεία είτε δηλώνουν εμφάνιση επιπλοκών όπως την επιδείνωση της νεφρικής λειτουργίας. Επιπροσθέτως, συμπέραναν ότι επί εφαρμογής ορθής και καθοδηγούμενης αγωγής, η εμφάνιση επιδείνωσης των δεικτών μυοκαρδιακής συσταλτικότητας VI και STR, συνήθως υποδεικνύουν ανάπτυξη ανεπάρκειας της αριστεράς κοιλίας. Οι δείκτες αυτοί κρίθηκαν ως οι πλέον πρώιμοι ανιχνευτές καρδιακής ανεπάρκειας είτε οφειλόταν σε βαλβιδοπάθεια είτε σε ισχαιμία απότοκης στεφανιαίας αθηρωμάτωσης.
Η καρδιογραφία αντίστασης στην αναπνευστική συμπτωματολογία
Η Καρδιογραφία αντίστασης είναι χρήσιμη στην διαφορική διάγνωση, στην διάγνωση, στην λήψη επειγουσών θεραπευτικών αποφάσεων και στην προγνωστική αξιολόγηση μιας μεγάλης σειράς περιπτώσεων όπου προεξάρχει η σημειολογία ή η συμπτωματολογία από το αναπνευστικό, όπως είναι η δύσπνοια ή η πνευμονική υπέρταση. Η ομάδα των Springfield και συν. οδηγήθηκε στο συμπέρασμα ότι η χρήση της καρδιογραφίας αντίστασης μπορεί με στατιστική βεβαιότητα να διακρίνει αν η δύσπνοια είναι καρδιακής ή μη καρδιακής αιτιολογίας. Στο εγχειρίδιο χρήσης της συσκευής που κυκλοφόρησε η CardioDynamics το 2001 εμπεριέχεται ο υπολογισμός της πίεσης ενσφήνωσης της πνευμονικής αρτηρίας, ως υπολογιζόμενη αλγοριθμικά. Έκτοτε χρησιμοποιήθηκε σε δεκάδες μελέτες σε ασθενείς με πνευμονική υπέρταση ή και σε ασθενείς με αυξημένες αγγειακές πνευμονικές αντιστάσεις, με μεγάλη στατιστική συμφωνία. Στην μελέτη των Chatziantoniou και συν επιβεβαιώθηκε η σημαντική προσφορά της μεθόδου ICG ως αλάνθαστου κριτήριου πρώτης διαφοροδιαγνωστικής προσέγγισης του δυσπνοϊκού ασθενούς.
Οι Ziegler και συν. αξιοποίησαν τον αναίμακτο αιμοδυναμικό προσδιορισμό της καρδιακής παροχής στην παρακολούθηση ασθενών ευρισκόμενων σε μηχανικό αερισμό και διαπίστωσαν σχεδόν ταυτόσημα ευρήματα εν σχέση με την επεμβατική μέθοδο της θερμοαραίωσης.
Η καρδιογραφία αντίστασης στην καρδιοχειρουργική
Η καρδιογραφία αντίστασης είναι πολλαπλώς χρήσιμη στην λήψη θεραπευτικών αποφάσεων κατά την περίοδο φροντίδας μετά από επέμβαση αορτοστεφανιαίας παράκαμψης. Επίσης, την ίδια θετική συνεισφορά μπορεί να παρουσιάσει σε ασθενείς νοσηλευόμενους σε μονάδες εντατικής θεραπείας και σε ασθενείς που υποβάλλονται σε αιμοκάθαρση, όπου πολύτιμος κρίνεται ο υπολογισμός του όγκου παλμού και η περιεκτικότητα σε υγρά της θωρακικής κοιλότητας. Σε ασθενείς δε που φέρουν βηματοδότη, επιπλέον διευκολύνεται η βελτιστοποίηση των παραμέτρων βηματοδότησης.
Οι Silver και συν. έδειξαν την σπουδαιότητα από την εφαρμογή της καρδιογραφίας αντίστασης σε ασθενείς που έφεραν συσκευή μηχανικής υποβοήθησης της αριστεράς κοιλίας. Στις μελέτες των Thangathurai και συν., των Roessler και συν., όπως και των Savino και συν., επιβεβαιώθηκε η σημασία της συνεχούς διεγχειρητικής αναίμακτης αιμοδυναμικής παρακολούθησης των ασθενών που υποβάλλονται σε ποικίλες χειρουργικές επεμβάσεις και ιδιαίτερα τονίστηκε η σπουδαιότητα στους ηλικιωμένους ασθενείς. Τόσο οι προαναφερόμενοι τρεις συγγραφείς όσο και οι Koerner και συν. και Feng και συν., αναγνώρισαν την σπουδαιότητα της χρήσης των αναίμακτων αιμοδυναμικών δεικτών ACI, VI και dz/dt στην διάγνωση της στεφανιαίας καρδιοπάθειας.
Σημαντικά χαμηλότερες παράμετροι συσταλτικότητας και ιδίως οι ACI και dz/dt παρατηρήθηκαν σε ασθενείς με γνωστή στεφανιαία καρδιοπάθεια, τόσο στην ηρεμία όσο και στην προσπάθεια, παρά σε άτομα που δεν έπασχαν από στεφανιαία νόσο. Το σημαντικότερο όμως διαφοροδιαγνωστικό στοιχείο είναι ότι μεταξύ των δυο ομάδων στεφανιαίων και μη ασθενών δεν βρέθηκαν σημαντικές διαφορές ως προς τον όγκο παλμού SV. Το συμπέρασμα από τις παρατηρήσεις αυτές είναι ότι οι δείκτες ACI και dz/dt αποτελούν την πρωιμότερη διαγνωστική προσέγγιση της στεφανιαίας νόσου, ιδίως όταν επισυμβαίνει δυσανάλογη πτώση των επιπέδων τους σε συνθήκες ελαφριάς παραγωγής σωματικού μόχθου.
Η καρδιογραφία αντίστασης στην εγκυμοσύνη
Η καρδιογραφία αντίστασης έχει αποδειχθεί πολύ χρήσιμη για την παρακολούθηση των μεταβολών των αιμοδυναμικών παραμέτρων του κυκλοφορικού συστήματος στις εγκυμονούσες γυναίκες. Επίσης πολύτιμος είναι ο ρόλος της σε νεογνά, σε βρέφη και σε παιδιά, αφού η μέθοδος αφ΄ ενός μεν μπορεί να χρησιμοποιηθεί με επιτυχία, αφ΄ εταίρου δε στερείται επιπλοκών, ενώ η διενέργεια καθετηριασμού πνευμονικής αρτηρίας σε αυτές τις ηλικίες είναι από δυσχερής έως αδύνατη. Λόγω της περιορισμένης επιφάνειας του σώματος, όταν εφαρμόζεται η μέθοδος ICG σε βρέφη ή σε νεογνά, χρησιμοποιείται διαφορετική διαμόρφωση τοποθέτησης των αισθητήρων της συσκευής και ταυτοχρόνως χρησιμοποιούνται ειδικά καλώδια. Σε αυτές τις περιπτώσεις οι δημοσιευμένες μελέτες δεν παρουσιάζουν έως σήμερα ομοφωνία συμπερασμάτων και ως εκ τούτου εγγύηση αξιοπιστίας των μετρήσεων δεν παρέχεται. Η εφαρμογή της μεθόδου στα βρέφη και ειδικά στα νοσηλευόμενα σε θερμοκοιτίδες θα πρέπει να γίνεται ως ενδεικτική χρήσιμων πληροφοριών μόνο και να μην εκλαμβάνονται οι τιμές των αιμοδυναμικών παραμέτρων ως στατιστικά ασφαλείς, έως ότου αναπτυχθούν και δημοσιευθούν νέοι επιβεβαιωμένοι αλγόριθμοι.
Η καρδιογραφία αντίστασης στην καρδιακή βηματοδότηση
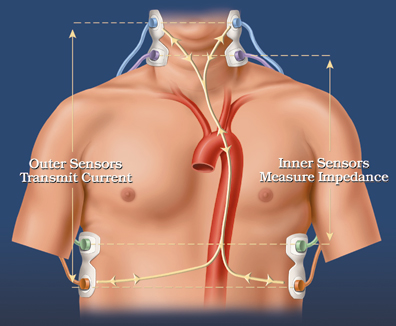
Μεγάλες προοπτικές φαίνεται πως ανοίγονται από την καθοδηγητική εφαρμογή της καρδιογραφίας αντίστασης για την επίτευξη βέλτιστων κολποκοιλιακών ρυθμίσεων σε βηματοδότες DDD, ενώ ήδη η μέθοδος καθιερώθηκε σαν ιδανικός αλγόριθμος για τους βηματοδότες CRT. Η ICG διαβιβάζει ένα μικρό ρεύμα υψηλής συχνότητας μέσω του θώρακα και στην συνέχεια υπολογίζει την αντίσταση. Αυτό το μικρό ρεύμα μπορεί να επηρεάσει μερικούς βηματοδότες που διαθέτουν ειδικές λειτουργίες ανίχνευσης. Μέχρι σήμερα έχει επιβεβαιωθεί ότι τα ηλεκτρικά σήματα της ICG παρεμβαίνουν μόνο στους «ελεγχόμενου ρυθμού ανταποκρινόμενους βηματοδότες» που συνήθως αποκαλούνται «minute ventilation pacemakers MVP». Αυτοί οι βηματοδότες ανιχνεύουν τα σήματα ηλεκτρικής αντίστασης (impedance) από τις αναπνευστικές κινήσεις προκειμένου να ρυθμίσουν την συχνότητα των καρδιακών ερεθισμάτων και μπορεί κατά λάθος να εκλάβουν την μεταβολή της αντίστασης από το σήμα της ICG ως αναπνευστικό σήμα. Ως εκ τούτου προκειμένου να εφαρμοστεί η μέθοδος σε βηματοδοτημένο ασθενή, πρέπει να έχει εξασφαλιστεί ότι ο βηματοδότης δεν είναι MVP.
Διαφορική διάγνωση της δύσπνοιας
Οι Springfield και συν. έδειξαν ότι η καρδιογραφία αντίστασης είναι χρήσιμο εργαλείο στην διαφοροδιαγνωστική προσπέλαση δυσπνοϊκών ασθενών. Οι ερευνητές αυτοί διαπίστωσαν σημαντικές διαφορές στον καρδιακό δείκτη CI, στην αναλογία του συστολικού χρόνου STR και στον δείκτη ταχύτητας VI. Συγκεκριμένα, στην ομάδα της δύσπνοιας καρδιογενούς αιτιολογίας ο μέσος CI ήταν 2,2 έναντι 3,1 της ομάδας μη καρδιογενούς δύσπνοιας, (ρ<0,0001), το μέσο STR βρέθηκε 0,52 έναντι 0,37 (ρ<0,01) και οι μέσες τιμές του VI ήταν 32,9 έναντι 42,7 (ρ<0,01), αντίστοιχα στις προαναφερόμενες ομάδες.
Θεραπευτική στρατηγική καθοδηγούμενη από αιμοδυναμικές παραμέτρους
Οι Albert και συν. συμπέραναν ότι η διαθεσιμότητα των αιμοδυναμικών παραμέτρων μπορεί να επηρεάσει ευμενώς την ακολουθούμενη θεραπεία. Στην μελέτη που πραγματοποίησαν με ασθενείς που είχαν χαμηλή καρδιακή παροχή CO, η συχνή παρακολούθηση της καρδιακής απόδοσης, αύξησε τον αριθμό των θεραπευτικών αποφάσεων, ενώ ταυτόχρονα ελάττωσε τον μέσο χρόνο νοσηλείας κατά δυο ημέρες.
Στην μελέτη ED-IMPACT αξιολογήθηκε η αιμοδυναμική συνεισφορά της καρδιογραφίας αντίστασης στην λήψη θεραπευτικών χειρισμών σε ασθενείς με δύσπνοια που αντιμετωπίστηκαν στο τμήμα επειγόντων περιστατικών. Διαπιστώθηκε ότι στο 24% αυτών των ασθενών απαιτήθηκε αλλαγή της θεραπευτικής στρατηγικής όταν λαμβάνονταν οι αιμοδυναμικές τιμές από την διενέργεια καρδιογραφίας αντίστασης, ενώ η αλλαγή θεραπευτικής στρατηγικής έγινε μόνο στο 11% των ασθενών όταν χρησιμοποιήθηκε ως κριτήριο το επίπεδο του εγκεφαλικού νατριουρητικού πεπτιδίου (brain natriuretic peptide, BNP). Οι συγγραφείς κατέληξαν στο συμπέρασμα ότι η καρδιογραφία αντίστασης πλεονεκτεί σαφώς έναντι του νατριουρητικού πεπτιδίου, ως προς την λήψη θεραπευτικών αποφάσεων.
Oι Taler και συν. στην μελέτη τους τόνισαν την αποτελεσματικότητα της καρδιογραφίας αντίστασης στην καθοδήγηση της αντιυπερτασικής θεραπείας στην ανθιστάμενη υπέρταση. Οι Yung και συν. επιβεβαίωσαν την ακρίβεια των αιμοδυναμικών τιμών της καρδιακής παροχής CO και του καρδιακού δείκτη CI που λήφθηκαν με την καρδιογραφία αντίστασης σε ασθενείς που έπασχαν από πνευμονική υπέρταση. Στην μελέτη τους συνέκριναν τις τιμές που λαμβάνονταν με τρεις μεθόδους, την καρδιογραφία αντίστασης (ICG), την μέθοδο της θερμοαραίωσης (TD) και την μέθοδο του Fick (F). Οι στατιστικές συσχετίσεις που έκαναν στην συνέχεια έδειξαν πολύ υψηλή σημαντικότητα και συγκεκριμένα βρέθηκαν οι εξής συσχετίσεις: ICG με F 0,84, TD με F 0,89 και ICG με TD 0,80.
Εκτίμηση της πνευμονικής συμφόρησης
Η καρδιογραφία αντίστασης μπορεί να εφαρμοστεί ως αιμοδυναμική παρακολούθηση κατά την διάρκεια της διουρητικής θεραπείας καθώς και κατά την εκκενωτική παρακέντηση του θώρακα (πλευροκέντηση) όπως και κατά την περικαρδιοκέντηση. Η περιεκτικότητα υγρών του θώρακα (Thoracic Fluid Content, TFC), είναι μέγεθος αντίστροφο της θωρακικής αντίστασης Ζ και σχετίζεται στενά με το συνολικό ποσό υγρών της θωρακικής κοιλότητας, τόσο το ενδοαγγειακό όσο και το εξωαγγειακό. Οι Peterson και συν. έδειξαν υψηλό βαθμό συσχέτισης μεταξύ του πλευριτικού υγρού που αφαιρείται με την πλευροκέντηση και την αλλαγή της αντίστασης του θώρακα. Παρόμοια ήταν και τα ευρήματα των Ebert και συν. οι οποίοι ανέδειξαν μια σχεδόν ιδανική γραμμική συσχέτιση μεταξύ των αλλαγών στην κεντρική φλεβική πίεση και των μεταβολών της συνολικής αντίστασης του θώρακα.
Παρακολούθηση μετά από ορθοτοπική μεταμόσχευση καρδιάς
Με τις αιμοδυναμικές παραμέτρους της καρδιογραφίας αντίστασης μπορεί να γίνει παρακλινική εκτίμηση ασθενών που έχουν υποβληθεί σε μεταμόσχευση καρδιάς. Σύμφωνα με την μελέτη των Nollert και Reichart, ελάττωση κατά 20% του δείκτη επιτάχυνσης (Acceleration Index, ACI) που αποτελεί ευαίσθητο δείκτη μυοκαρδιακής συσταλτικότητας, έχει ευαισθησία 71% και ειδικότητα 100% στην διάγνωση απόρριψης καρδιακού μοσχεύματος. Οι ίδιοι συγγραφείς συμπέραναν επίσης ότι η παρακολούθηση των μεταμοσχευμένων με την καρδιογραφία αντίστασης μπορεί να οδηγήσει σε σημαντική μείωση τον αριθμό των απαιτούμενων καρδιακών βιοψιών.
Καρδιακή ανεπάρκεια
Τα στοιχεία των αιμοδυναμικών παραμέτρων που λαμβάνονται από την καρδιογραφία αντίστασης είναι πολύ χρήσιμα στην διάγνωση και την θεραπεία των ασθενών με καρδιακή ανεπάρκεια καθώς και στην εξαγωγή ασφαλούς πρόγνωσης. Οι Albert και συν. απέδειξαν την χρησιμότητα της μεθόδου σε περιπτώσεις μη αντιρροπούμενης καρδιακής ανεπάρκειας. Χάρις στην καρδιογραφία αντίστασης οι κίνδυνοι που σχετίζονται με τον καθετηριασμό της πνευμονικής αρτηρίας, όπως είναι η λοίμωξη, η διάτρηση και η πρόκληση αρρυθμίας, μπορούν να αποφευχθούν. Επιπρόσθετα πλεονεκτήματα αυτής της μη επεμβατικής μεθόδου είναι το χαμηλό κόστος και η εξοικονόμηση χρόνου τόσο για το ιατρικό όσο και για το νοσηλευτικό προσωπικό.
Εξάλλου, ο μη επεμβατικός υπολογισμός του όγκου παλμού (stroke volume, SV), έχει ιδιαίτερη σημασία για ασθενείς ευρισκόμενους σε ενδοφλέβια φαρμακοθεραπεία συμπεριλαμβανομένων των ινοτρόπων.
Οι Vijayaraghavan και συν. απέδειξαν τον προγνωστικό ρόλο των αιμοδυναμικών παραμέτρων που λαμβάνονται με την καρδιογραφία αντίστασης σε ασθενείς με χρόνια καρδιακή ανεπάρκεια, καθώς και την ισχυρή θετική συσχέτιση των μεταβολών αυτών των παραμέτρων με την λειτουργική κλάση της καρδιακής ανεπάρκειας καθώς και με την ποιότητα ζωής. Χάρη στην μέθοδο αυτή είναι δυνατό να διερευνηθεί η επίδραση των φαρμάκων στις αιμοδυναμικές παραμέτρους, να αξιολογηθεί η αστάθεια ή η σταθερότητα του κυκλοφορικού συστήματος, καθώς και να επιλεγεί η κατάλληλη ή η πιο έγκαιρη στιγμή για την φαρμακευτική παρέμβαση ανάσχεσης των κυκλοφορικών διαταραχών ή πρόληψης της αιμοδυναμικής κατάρριψης.
Τα πλέον κλασσικά παραδείγματα φαρμακευτικής καθοδήγησης είναι η χορήγηση β- αναστολέα, η χορήγηση αναστολέα του μετατρεπτικού ενζύμου της αγγειοτενσίνης, η απόφαση για την κατάλληλη στιγμή έναρξης χορήγησης κατεχολαμινών επί καρδιακής κάμψης και ο καθορισμός της χορηγούμενης δοσολογίας όπως και η παρακολούθηση της αποτελεσματικότητας της ακολουθούμενης θεραπείας σε περιπτώσεις μη αντιρροπούμενης καρδιακής ανεπάρκειας. Σε πάρα πολλές κλινικές μελέτες η καρδιογραφία αντίστασης συγκρίθηκε με τις επεμβατικές αιμοδυναμικές τεχνικές της θερμοαραίωσης και της μεθόδου του Fick, όπως και με τις αναίμακτες ή ημιεπεμβατικές τεχνικές της διοισοφάγειας υπερηχογραφίας. Σε όλες αυτές τις συγκριτικές μελέτες βρέθηκε υψηλός βαθμός στατιστικής συσχέτισης μεταξύ των τιμών των αιμοδυναμικών παραμέτρων που εξάγονται με την καρδιογραφία αντίστασης και αυτών που συνάγονται από την εφαρμογή επεμβατικών ή αναίμακτων ημιεπεμβατικών τεχνικών.
Οι Drazner και συν. μελέτησαν μια μεγάλη ομάδα ασθενών που έπασχαν από σοβαρού βαθμού καρδιακή ανεπάρκεια και υποβλήθηκαν σε καθετηριασμό της πνευμονικής αρτηρίας. Σε αυτούς τους ασθενείς συνέκριναν τα αιμοδυναμικά ευρήματα που ελήφθησαν μετά τον καθετηριασμό με αυτά που έλαβαν με την τεχνική της καρδιογραφίας αντίστασης. Διαπίστωσαν ότι η συσχέτιση των τιμών του όγκου παλμού (SV) όπως εκτιμήθηκε με την καρδιογραφία αντίστασης και με την μέθοδο του Fick, ήταν σε στατιστική συμφωνία με την σύγκριση μεταξύ της θερμοαραίωσης και της μεθόδου του Fick. Οι συγγραφείς αυτοί έδειξαν ότι η συσχέτιση Pearson μεταξύ της καρδιογραφίας αντίστασης και της θερμοαραίωσης ήταν 0,76 για την καρδιακή παροχή (CO) και 0,64 για τον καρδιακό δείκτη (CI). Στην εργασία εξάλλου των Albert και συν. οι αντίστοιχες συσχετίσεις βρέθηκαν 0,89 και 0,82 αντιστοίχως και τοιουτοτρόπως όλοι οι συγγραφείς μπόρεσαν να ισχυριστούν ότι η καρδιογραφία αντίστασης έχει αποδεδειγμένη κλινική χρησιμότητα στην καρδιακή ανεπάρκεια και ότι ο ρόλος της είναι από πολύτιμος έως αναντικατάστατος στην μη αντιρροπούμενη ή στην οριακά αντιρροπούμενη μορφή της.
Άλλες μέθοδοι υπολογισμού αιμοδυναμικών παραμέτρων
Σε αντίθεση με τα προαναφερόμενα υπάρχουν αρκετές μελέτες που δεν επιβεβαίωσαν την υψηλή στατιστική συσχέτιση μεταξύ καρδιογραφίας αντίστασης και των επεμβατικών τεχνικών. Οι Engoren και Barbee δήλωσαν ότι η μέτρηση του όγκου παλμού μέσω της καρδιογραφίας αντίστασης, της θερμοαραίωσης και της μεθόδου του Fick δεν είναι συγκρίσιμες σε μια ετερογενή ομάδα ασθενών ευρισκόμενων σε βαριά κλινική κατάσταση. Σε αυτές τις περιπτώσεις η μέτρηση του όγκου παλμού (SV) με την καρδιογραφία αντίστασης δεν ήταν αρκετά ακριβής ώστε να μπορέσει να αντικαταστήσει την μέθοδο της θερμοαραίωσης. Η μέτρηση του όγκου παλμού μπορεί να προσδιοριστεί με την υπερηχογραφία και ιδίως με την διοισοφάγεια τεχνική με καλή συσχέτιση συγκρινόμενη με τις επεμβατικές τεχνικές. Όμως, σε σχέση με την καρδιογραφία αντίστασης, η υπερηχογραφία είναι πιο χρονοβόρα, πιο δαπανηρή, ημιεπεμβατική και απαιτεί κατάλληλο εργαστήριο όπως και κατάλληλα εκπαιδευμένο προσωπικό.
Οι Parrot και συν. συνέκριναν την καρδιογραφία αντίστασης με την υπερηχογραφία και συμπέραναν ότι η πρώτη μέθοδος εντόπιζε αλλαγές στη απόδοση της καρδιάς πιο εύκολα, πιο πρώιμα και με ασήμαντο οικονομικό κόστος. Οι συγγραφείς αυτοί απέδειξαν μεγάλο βαθμό συσχέτισης μεταξύ των αλλαγών στις παραμέτρους CI (καρδιακός δείκτης) και STR (αναλογία συστολικού χρόνου) και του υπερηχογραφικού κλάσματος εξώθησης (EF) και συγκεκριμένα οι συσχετίσεις που βρέθηκαν ήταν 0,85 μεταξύ του CI και του EF και -0,73 μεταξύ του STR και του EF.
Η εκτίμηση της καρδιακής παροχής μέσω της άμεσης μεθόδου του Fick θεωρείται ως η πιο ακριβής μέθοδος, παρόλο που είναι πολύ χρονοβόρος και περιλαμβάνει την αναγκαιότητα λήψης δειγμάτων αίματος από την πνευμονική αρτηρία καθώς και λήψης περιφερικού αρτηριακού αίματος. Αντίθετα, η έμμεση μέθοδος κατά Fick χρησιμοποιεί την μέθοδο της παλμικής οξυμετρίας αντί την λήψης αίματος, αν και εξακολουθεί ακόμα να προτιμάται σε περιπτώσεις δυσχέρειας καθετηριασμού της πνευμονικής. Όμως είναι γνωστό ότι η μέθοδος του Fick είναι μη εφαρμόσιμη ή και άχρηστη επί ύπαρξης πνευμονικών νοσημάτων.
Η μέθοδος που προτιμάται σήμερα περισσότερο είναι η θερμοαραίωση, δεδομένου ότι πολύ συχνά συνυπάρχουν αναπνευστικά νοσήματα, ιδίως σε υπερήλικες ή σε βαριές περιπτώσεις καρδιακής ανεπάρκειας. Η μέθοδος της θερμοαραίωσης έχει και αυτή τους δικούς της όμως περιορισμούς. Είναι γνωστό ότι κατά την θερμοαραίωση η εξαγόμενη τιμή της καρδιακής παροχής παρουσιάζει μεταβλητότητα που μπορεί να κυμαίνεται από 5% έως και 20%. Για τον λόγο αυτό και προς περιορισμό του στατιστικού σφάλματος, προκειμένου να εξαχθεί η καρδιακή παροχή η μέθοδος πραγματοποιείται τρεις φορές και υπολογίζεται ο μέσος όρος των τιμών, εφ΄ όσον οι λαμβανόμενες τιμές δεν ξεπερνούν μεταξύ τους μια διασπορά της τάξης του 10%. Όμως τόσο η θερμοαραίωση όσο και η μέθοδος του Fick είναι πράξεις δαπανηρές και χρονοβόρες και ενέχουν τους δυνητικούς κινδύνους και τις ενδεχόμενες επιπλοκές του καθετηριασμού της πνευμονικής αρτηρίας.
Είναι ευκολότερος ο υπολογισμός του όγκου παλμού μέσω της καρδιογραφίας αντίστασης από ότι με την μέθοδο της θερμοαραίωσης, ενώ ταυτόχρονα πραγματοποιείται πιο γρήγορα, πιο οικονομικά και χωρίς τον κίνδυνο λοίμωξης ή τους άλλους κινδύνους του καθετηριασμού της πνευμονικής. Επιπροσθέτως, η καρδιογραφία αντίστασης επιτρέπει την παρακολούθηση της τιμής του όγκου παλμού και της καρδιακής παροχής σε συνεχή χρονική ροή, σε αντίθεση με την θερμοαραίωση, στην οποία πραγματοποιούνται απλές και πεπερασμένου χρόνου μετρήσεις, με την ταυτόχρονη απαίτηση ένεσης υγρών, πράξης που προσθέτει επιβάρυνση στους ήδη επιβαρυμένους ασθενείς.
Στην βιβλιογραφία μπορούμε να βρούμε πολλές εργασίες που εισηγούνται ότι η θεραπεία ασθενών με καρδιακή ανεπάρκεια έχει καλύτερα αποτελέσματα όταν στηρίζεται στα ευρήματα που λαμβάνονται από τον καθετηριασμό της πνευμονικής. Επίσης μπορούμε να βρούμε πληθώρα εργασιών που εισηγούνται αντίθετα συμπεράσματα, θέτοντας εύλογα ερωτήματα για την χρησιμότητα, την ασφάλεια και τα ενδεχόμενα οφέλη από την χρήση αιματηρών αιμοδυναμικών τεχνικών. Οι εργασίες αυτές τονίζουν ότι οι επεμβατικές τεχνικές ακόμη και όταν βελτιώνουν την αποτελεσματικότητα της θεραπείας, αυξάνουν την συχνότητα των επιπλοκών και το απορρέον συνολικό κόστος, οδηγώντας σε μικρή ή και μηδενική συνολική ωφέλεια για τον ασθενή. Οι Silver και συν. τόνισαν το υψηλό κόστος του καθετηριασμού της πνευμονικής και πρότειναν την αντικατάσταση της μεθόδου από την καρδιογραφία αντίστασης (ICG). Σε παρόμοιες διαπιστώσεις και ανάλογες συστάσεις κατέληξε και η ανασκόπηση του Hendrickson.
Οικονομικές όψεις της καρδιογραφίας αντίστασης
Το κόστος της καρδιογραφίας αντίστασης έγκειται στην δαπάνη αγοράς της συσκευής και στο επιπρόσθετο κόστος από την αγορά των ηλεκτροδίων τα οποία έχουν αναλώσιμο χαρακτήρα και χαμηλή τιμή αγοράς. Δεν υπάρχουν επιπρόσθετα κοστολόγια. Δεν υπάρχουν κίνδυνοι κατά την εκτέλεση της εξέτασης ούτε πιθανότητα επιπλοκών μετά την ολοκλήρωση της μελέτης. Τα αποτελέσματα της αιμοδυναμικής μελέτης λαμβάνονται αμέσως μετά την ολοκλήρωση της εξέτασης, επιταχύνοντας την εξαγωγή ασφαλούς διάγνωσης και έναρξης της καταλληλότερης φαρμακευτικής αγωγής ή τροποποίησης αυτής και με αυτόν τον τρόπο συντομεύει η διάρκεια της νοσηλείας, επιφέροντας περαιτέρω μείωση του κόστους.
Σύμφωνα με την μελέτη των Clancy και συν. η αρχική βασική εξοικονόμηση χρημάτων από την εφαρμογή της καρδιογραφίας αντίστασης για αιμοδυναμική προσπέλαση αντί της διενέργειας επεμβατικού καθετηριασμού της πνευμονικής, ξεπερνάει τα 600 δολάρια ανά ασθενή. Επιπροσθέτως, η εξοικονόμηση χρόνου από το ιατρικό και νοσηλευτικό προσωπικό καθώς και η δεδομένη αποφυγή της θεραπείας των επιπλοκών του πνευμονικού καθετηριασμού, αντιστοιχούν σε περαιτέρω σημαντικές μειώσεις από την συνολική αποτίμηση του κόστους, που όμως αν και είναι σίγουρες και σημαντικές, δεν είναι δυνατόν να προσδιοριστούν επακριβώς και με στατιστικές μεθόδους, αφού αναφέρονται σε τυχαία γεγονότα ποικίλης διασποράς και απροσδιόριστης συχνότητας.
Η ένδειξη καθετηριασμού της πνευμονικής
Τα τελευταία χρόνια όλο και περισσότερο τίθεται το ερώτημα αν ο καθετηριασμός της πνευμονικής εξακολουθεί να είναι χρήσιμος, με δεδομένους τους κινδύνους επιπλοκών που εγκυμονούνται και που στην βιβλιογραφία αναφέρονται ολοένα και με μεγαλύτερη συχνότητα. Πολλές μελέτες έδειξαν ότι η συνήθης χρήση καθετήρων πνευμονικής αρτηρίας σε ασθενείς νοσηλευόμενους σε κρίσιμη κατάσταση, συνδυάζεται με αυξημένη θνητότητα και αυξημένο κόστος της θεραπείας.
Στην μελέτη των Chittock και συν. βρέθηκε ότι η χρήση ενός καθετήρα πνευμονικής αρτηρίας μείωσε την θνητότητα σε ασθενείς νοσηλευόμενους σε σοβαρή κατάσταση, ενώ αντίθετα σε ασθενείς που δεν ευρίσκονταν σε βαριά κατάσταση συσχετίστηκε με αξιόλογη αύξηση της θνητότητας. Το 1997 η Ιατρική Εταιρεία Επείγουσας Φροντίδας ( The Society of Critical Care Medicine, SCCM) εξέφρασε την άποψη ότι η διενέργεια καθετηριασμού της πνευμονικής αρτηρίας σε πάσχοντες από καρδιακή ανεπάρκεια ήταν αμφίβολης αποτελεσματικότητας και εισηγήθηκε ότι ήταν αναγκαία η έναρξη τυχαιοποιημένων μελετών, προκειμένου να αποσαφηνιστεί αν τα οφέλη του εν λόγω καθετηριασμού υπερβαίνουν τους κινδύνους ή τις επιπλοκές του.
Με βάση τις εισηγήσεις της SCCM σχεδιάστηκε και προχωρά η πολυκεντρική τυχαιοποιημένη μελέτη ESCAPE (Evaluation Study of Congestive Heart Failure and Pulmonary Artery Catheterisation Effectiveness). Η μελέτη αυτή έχει σχεδιαστεί έτσι ώστε να γίνει εκτίμηση της αποτελεσματικότητας του καθετηριασμού της πνευμονικής ως μεθόδου εκτίμησης της συμφορητικής καρδιακής ανεπάρκειας. Ταυτόχρονα έχει διαμορφωθεί μια υποομάδα βιοαντίστασης (bioimpedance subgroup), όπου μελετάται η χρησιμότητα της καρδιογραφίας αντίστασης σε ασθενείς με προχωρημένη καρδιακή ανεπάρκεια.
Ο καθετηριασμός της πνευμονικής αρτηρίας είναι γνωστό ότι ενέχει μεγάλη ποικιλία επιπλοκών, μεταξύ των οποίων στην βιβλιογραφία αναφέρονται τα εξής: τρώση ή σχάση του τοιχώματος της πνευμονικής αρτηρίας, πνευμοθώρακας, εμβολή από αέρα, σηψαιμία, φλεβοθρόμβωση, πνευμονική εμβολή, ενδοκαρδίτις, αρρυθμίες και αύξηση της θνητότητας. Επειδή έως σήμερα δεν υπήρξαν προοπτικές μελέτες που να αποδεικνύουν τα πλεονεκτήματα του καθετηριασμού, πολλοί Ιατροί εγκατέλειψαν την μέθοδο. Επιπλέον, με την πάροδο του χρόνου, ολοένα και λιγότεροι από τους βαρέως πάσχοντες ασθενείς που παρουσιάζουν επιδεινούμενη καρδιακή ανεπάρκεια νοσηλεύονται σε μονάδες εντατικής θεραπείας (ΜΕΘ), όπου είναι δυνατός ο καθετηριασμός της πνευμονικής. Σε αυτούς τους ασθενείς η καρδιογραφία αντίστασης μπορεί να παράσχει τα αναγκαία αιμοδυναμικά στοιχεία σε οποιοδήποτε τμήμα του Νοσοκομείου και αν νοσηλεύονται.
Με βάση τα ανωτέρω συμπεραίνεται ότι η καρδιογραφία αντίστασης είναι μέθοδος απλούστερη, ταχύτερη, σημαντικά ασφαλέστερη από κάθε άλλη ως μη επεμβατική και δεν επιβαρύνει καθόλου τον ασθενή, ενώ ταυτόχρονα εγγυάται στατιστική αξιοπιστία.
Τα τελευταία χρόνια και συγκεκριμένα το 2005 και το 2007, έχουν ολοκληρωθεί δυο πολυκεντρικές μελέτες που αφορούν την εφαρμογή της καρδιογραφίας αντίστασης στην διαχείριση ασθενών με χρόνια καρδιακή ανεπάρκεια. Η πρώτη μελέτη είναι η PREDICT (Prospective Evaluation and Identification of Decompensation by Impedance Cardiography Test), όπου μελετάται προοπτικά η πρόγνωση της χρόνιας καρδιακής ανεπάρκειας, στηριζόμενη στους αιμοδυναμικούς δείκτες της καρδιογραφίας αντίστασης. Η δεύτερη μελέτη είναι η BIG (BioImpedance cardioGraphy), που αποτελεί μέρος της μεγάλης μελέτης ESCAPE (Evaluation Study of Congestive Heart Failure and Pulmonary Artery Catheterisation Effectiveness) και όπου τα αιμοδυναμικά ευρήματα παραβάλλονται με τα αντίστοιχα του καθετηριασμού. Τα αποτελέσματα αυτών των μελετών που ήδη έχουν δημοσιευθεί, υποδεικνύουν με πολύ συγκεκριμένο τρόπο τον σημαντικό ρόλο της καρδιογραφίας αντίστασης στην φαρμακευτική και γενικότερη διαχείριση των ασθενών με καρδιακή ανεπάρκεια.
Περιορισμοί της καρδιογραφίας αντίστασης
Τα αποτελέσματα που λαμβάνονται με την καρδιογραφία αντίστασης μπορεί να εμπεριέχουν ανακριβείς τιμές στις ακόλουθες περιπτώσεις:
1. Όταν συνυπάρχει σημαντική ανεπάρκεια αορτής. Στην περίπτωση της σημαντικής ανεπάρκειας της αορτής μια σημαντική ποσότητα αίματος ρέει πίσω προς την αριστερά κοιλία κατά την διάρκεια της πρώιμης διαστολής. Αν και το αίμα αυτό εξωθείται έξω από την καρδιά κατά την συστολή, αυτό τελικά δεν ρέει προς την περιφέρεια και τοιουτοτρόπως μειώνει την πραγματική καρδιακή παροχή. Η ICG εκτιμά τον πλήρη όγκο παλμού και επομένως υπερεκτιμά την πραγματική καρδιακή παροχή, αφού συνυπολογίζεται ο επιστρεφόμενος όγκος αίματος. Οι δείκτες όμως συσταλτικότητας ACI και VI υπολογίζονται σωστά, αφού δεν επηρεάζονται από την παλίνδρομη ροή. Οι Schieken και συν. πρότειναν μέθοδο προσδιορισμού του παλινδρομούντος όγκου αίματος από την ανάλυση της κυματομορφής του ICG κύματος. Παρόλα ταύτα η μέθοδος που πρότειναν αν και τεκμηριωμένη δεν είναι κλινικά εύχρηστη.
2. Όταν συνυπάρχει βαριά στένωση αορτής. Όταν υπάρχει βαριά στένωση αορτής το αλγοριθμικό πρότυπο βάσει του οποίου αξιολογείται η εξώθηση του αίματος δεν υφίσταται, με αποτέλεσμα να υποεκτιμάται σημαντικά ο πραγματικός όγκος παλμού.
3. Μειωμένη αορτική ενδοτικότητα. Η ενδοτικότητα είναι η διατασιμότητα της αορτής, η οφειλόμενη στις αλλαγές της πίεσης του αίµατος. Κανονικά, σε αντίθεση µε τις πιο περιφερειακά ευρισκόµενες αρτηρίες, η θωρακική αορτή έχει µια πολύ υψηλή ενδοτικότητα. Το αποτέλεσµα αυτής της υψηλής ενδοτικότητας είναι ότι η αύξηση της πίεσης κατά τη διάρκεια της εξώθησης του αίµατος είναι χαµηλή. Το καρδιακό έργο παραµένει επίσης χαµηλό. Αυτή η λειτουργία είναι επίσης γνωστή ως Windkessel λειτουργία της αορτής. Η υψηλή ενδοτικότητα προκαλεί µία χαµηλή ταχύτητα του σφυγµικού κύµατος. Επομένως, το αίµα που εξωθείται έξω από την αριστερά κοιλία παραµένει στη θωρακική αορτή για έναν πιο παρατεταμένο χρόνο. Αυτή είναι η βάση που η ICG µπορεί να χρησιμοποιηθεί για την µέτρηση του όγκου παλµού της καρδιάς. Για τον προσδιορισµό της µέγιστης συστολικής ταχύτητας εξώθησης (dZmax = C- σηµείο), το εξωθούµενο αίµα από την κοιλία πρέπει να παραµείνει στο µετρούµενο τµήµα έως ότου επιτευχθεί η µέγιστή του ταχύτητα εξώθησης ( C- σηµείο). Όσο σκληρότερη είναι η αορτή, δηλαδή όσο πιο μειωµένη είναι η ενδοτικότητά της ή/και πιο καθυστερημένα συμβαίνει η µέγιστη συστολική ταχύτητα εξώθησης ως προκαλούμενη από µία σημαντικά µειωµένη συσταλτικότητα της καρδιάς, τόσο περισσότερο αίµα έχει ήδη φύγει από το µετρούµενο τµήµα, γεγονός το οποίο προκαλεί χαμηλότερο ύψος της καµπύλης της ICG. Συνεπώς, η καρδιακή παροχή και οι σχετιζόμενες µε αυτήν παράμετροι όπως οι ACI και VI, θα υποτιμηθούν. Δηλαδή η πραγματική καρδιακή παροχή θα είναι υψηλότερη από την µετρηθείσα τιµή. Σε μερ4ικές περιπτώσεις βαριάς ή χρονίζουσας υπέρτασης, η ενδοτικότητα της αορτής είναι συνήθως µειωµένη. Όµως είναι γνωστόν ότι η σχέση µεταξύ της αρτηριακής πίεσης και της ενδοτικότητας της αορτής είναι µη γραµµική. Γενικά, όσο υψηλότερη η αρτηριακή πίεση, τόσο περισσότερη είναι ήδη η τοιχωματική τάση της αορτής και τόσο μικρότερη η ενδοτικότητά της. Οι ακόλουθες παθολογικές µεταβολές ή παθήσεις είτε υπάρχουν αυτοτελώς είτε συνυπάρχουν, µπορούν να προξενήσουν σημαντική µείωση της αορτικής ενδοτικότητας:
1. Σημαντικού βαθμού αθηροσκλήρωση
2. Υψηλή µέση αρτηριακή πίεση (όσο µεγαλύτερη είναι η τοιχωματική τάση του αρτηριακού τοιχώματος, τόσο χαμηλότερη είναι η ενδοτικότητά του)
3. Προσθετική επέμβαση στην αορτική βαλβίδα ή στην ανιούσα αορτή
Οι περιορισµοί που προπεριγράφονται µπορούν να συναντηθούν συνήθως στις ακόλουθες οµάδες ασθενών:
• ηλικιωμένοι ασθενείς µε σημαντικού βαθµού αθηροσκλήρωση
• ασθενείς µε υψηλό βαθµό υπέρτασης ή με υπέρταση χρονολογούμενη από ετών
• ασθενείς µε πολύ κακή αριστερή καρδιακή λειτουργία, όπως ασθενείς ευρισκόμενοι σε σηπτικό shook
Στην κλινική πρακτική, οι προπεριγραφείσες παθολογικές µεταβολές µπορούν να αναγνωριστούν µόνο σε πολύ προχωρημένα στάδια των παθήσεων, µε βάση την µορφή της ICG καµπύλης, όπου κανένα σαφές συστολικό κύµα δεν ανευρίσκεται. Επομένως, στις περιπτώσεις τέτοιων ασθενών, τα αποτελέσµατα της καρδιογραφίας αντιστάσεων πρέπει να αξιολογούνται µε πολύ προσοχή. Ειδικότερα, αν ο ασθενής έχει ένα πολύ χαµηλό όγκο παλµού ή πολύ μικρό καρδιακό δείκτη (ως υποτιμώμενος), ο οποίος δεν ανταποκρίνεται στο ιστορικό και στην κλινική εικόνα, πρέπει να υποτεθεί ότι η ακρίβεια της ICG έχει μειωθεί λόγω των αναφερθέντων περιορισµών της µεθόδου. Κάτω απ΄ αυτές τις συνθήκες, οι απόλυτες τιµές δεν µπορούν να χρησιμοποιηθούν για διαγνωστικούς σκοπούς. Όµως οι χρονικές παράμετροι και οι μεταβολές των παραμέτρων σε διαδοχικές εκτιμήσεις µπορούν να παράσχουν χρήσιµες κλινικές πληροφορίες.
4. Όταν κατά την διενέργεια της εξέτασης υπάρχει σημαντικού βαθμού αρτηριακή υπέρταση με μέση αρτηριακή πίεση >130 mmHg (MAP>130mmHg). Ο προσδιορισµός της ταχύτητας του σφυγµικού κύµατος στην αορτή επιτρέπει την αξιολόγηση του αγγειακού συστήµατος ενός ασθενή (επίπεδο αρτηριοσκληρωτικών αλλαγών) και µπορεί να εξεταστεί µε την ICG, αφού η αρτηριακή πίεση συμπεριλαμβάνεται στις παραμέτρους, καθώς η ταχύτητα του σφυγµικού κύµατος εξαρτάται επίσης απ΄ αυτήν. Όσο υψηλότερη η αρτηριακή πίεση, τόσο χαμηλότερη η ενδοτικότητα των αγγείων και τόσο υψηλότερη η ταχύτητα του σφυγµικού κύµατος
5. Όταν το ύψος του εξεταζόμενου είναι μικρότερο από 120 cm ή μεγαλύτερο από 230cm.
6. Όταν το βάρος του ασθενούς είναι μικρότερο από 30 Kgr ή μεγαλύτερο από 155 Kgr.
7. Όταν στον εξεταζόμενο έχει τοποθετηθεί μπαλόνι ενδοαορτικής αντλίας για αιμοδυναμική υποστήριξη, διότι τότε τροποποιείται το αυτόχθον σφυγμικό κύμα.
8. Σε ασθενείς που φέρουν μόνιμο βηματοδότη με αισθητήρα που αναγνωρίζει τον ρυθμό των αναπνευστικών κινήσεων ανά λεπτό (sensor responsible for minute ventilation rate). Η βηματοδοτική συχνότητα αυτών των ασθενών μπορεί να αυξηθεί από το ηλεκτρικό σήμα που διοχετεύεται κατά την διενέργεια καρδιογραφίας αντίστασης, γι΄ αυτό πρέπει να γίνεται απενεργοποίηση του εν λόγω προγράμματος όταν προγραμματίζεται η εξέταση.
Σε ασθενείς με κολπική μαρμαρυγή ή πολυάριθμες έκτακτες συστολές, μια σημαντική επίταση του αρρυθμιολογικού φαινόμενου κατά την εκτέλεση της εξέτασης μπορεί να επηρεάσει το σήμα της καρδιογραφίας αντίστασης και να κάνει αδύνατη την αιμοδυναμική διερεύνηση.
Βιβλιογραφία
1. Brown CV, Shoemaker WC, Wo CC, Chan L, Demetriades D. Is noninvasive hemodynamic monitoring appropriate for the elderly critically injured patient? J Trauma, 2005; 58: 102-107.
2. Neath SX, Lazio L, Guss DA. Utility of impedance cardiography to improve physician estimation of hemodynamic parameters in the emergency department. Congest Heart Fail, 2005; 11: 17 -20.
3. Springlielg CL, Sebat F, Johnson D, Lengle S, Sebat C. Utility of impedance cardiography to determine cardiac vs noncardiac cause of dyspnea in emergency department. Congest Heart Fail. 2004; 10 (suppl 2): 14-16.
4. Antonelli M, Levy M, Andrews PJ, Chastre J, Hudson LD, Manthous C, Meduri GU, et all. Hemodynamic monitoring in shock and implications for management. International Consensus Conference, Paris , France
5. Payen D, Gayat E. Which general intensive care unit patients can benefit from placement of a pulmonary artery catheter? Crit Care 2006; 10 Suppl 3: S 7.
6. Ronkin MA. Rheoencephalography. In Ronkin MA, Ivanov LB, editors. Rheography in clinical practice. Moscow
7. Sharman DL, Gomes CP, Rutherford JP. Improvement in blood pressure control with impedance cardiography-guided pharmacologic decision making. Congest Heart Fail, 2004; 10: 54 -58.
8. Milzman D, Hogan C. Continuous noninvasive cardiac output monitoring quantifies acute congestive heart failure in the emergency department. Crit Care Med, 1997; 25: A47 (abstract).
9. Knauth M, Ordovas K, Higgins C. Magnetic Resonance Imaging in adults with congenital heart disease. Semin Roentgenol 2008; 43: 246 – 58.
10. Brown JM. Use of echocardiography for hemodynamic monitoring. Crit Care Med 2002; 30: 1361 – 1364.
11. Germano G, Kiat H, Kavanagh PB, Moriel M, Mazzanti M, Su HT, et al. Automatic quantification of ejection fraction from gated myocardial perfusion SPECT. The Journal of Nuclear Medicine, 1995; 36(11): 2138 – 2147.
12. Buell JC. A practical, cost-effective, noninvasive system for cardiac output and hemodynamic analysis. American Heart Journal 1988; 116(2): 657-66.
13. Fejfar Z, Zalic F. Clinical value of impedance plethysmography. Cas Lek Cesk 1955; 95(11): 282-90.
14. Kuicek WG, Krnegis JN, Patterson RP, Witsoe DA, Mattson RH. Development and evaluation of an impedance cardiac output system. Aerospace Med 1996; 37(12): 1208-1212.
15. Pranulis M. Impedance cardiography (ICG) noninvasive hemodynamic monitoring provides as opportunity to deliver cost effective quality care for patients with cardiovascular disorders. Journal of Cardiovascular Management 2000; 11(3): 13-18.
16. Ranuci M. Which cardiac surgical patients can benefit from placement of a pulmonary artery catheter? Crit Care 2006; 10 Suppl 3 : S 6.
17. Melc F, Buhre W, Hanekop G, Tirilomis T, Hilgers R, Sonntag H. Comparison of continuous cardiac output measurements in patients after cardiac surgery. J Cardiothorac Vasc Anesth 2003; 17: 211 – 216.
18. Hofer CK, Zollinger A. Less invasive cardiac output monitoring: characteristics and limitations. In: Vincent JL (editor) 2006, Yearbook of Intensive Care and Emergency Medicine. Spinger 2007; 162 – 175.
19. Magder S. Cardiac output. Tobin MJ (editor). In: Principles and practice of Intensive Care Monitoring. McGraw Hill 1998, pp: 797-810.
20. Strobeck J, Silver M. Beyond the four quadrants: the critical and emerging role of impedance cardiography in heart failure. Congest Heart Fail, 2004; 10(suppl 2): 1-6.
21. Siebert J. Ocena watrosci klinicznej badania ukladu krazenia i pluc za pomoca technik bio-impedan-cyjnych. Rozprawa habilitacyjna. Wydzial Lekarski, AMG, Gdanssk 2000: 1333.
22. Osypka MJ, Bernstein DP. Electrophysiologic principles and theory of stroke volume determination by thoracic electrical bioimpedance. AACN Clin Iss, 1999; 10: 385-395.
23. BioZ ICG Monitor User Manual. CardioDynamics, San Diego , CA
24. Greenberg BH, Hermann DD, Pranulis MF, Lazio L, Cloutier D. Reproducibility of impedance cardiography hemodynamic measures in clinically stable heart failure patients. Congest Heart Fail, 2000; 6: 19 -26.
25. Engoren M, Barbee D. Comparison of cardiac output determinate by bioimpedance, thermodilution, and the Fick method. Am J Crit Care, 2005; 14: 40 -45.
26. Ito H, Yamakoshi K, Yamada A. Physiological and fluid-dynamic investigation of the thoracic impedance plethysmography method for measuring cardiac output: Part II. Analysis of thoracic impedance wave by perfusing dog. Med Biol Eng, 1976; 14: 373.
27. Thomsen A. Impedance cardiography. Is the output from the tight or left ventricle measured? Int Care Med, 1979; 5: 206.
28. Lababidi Z, Ehmke A, Durin R, Leaverton P, Laurel R. The first derivative thoracic impedance cardiogram. Circulation, 1970; 41: 651-658.
29. Hubbard W, Fish D, McBrien D. The use of impedance cardiography in heart failure. Int J Cardiol, 1986; 12: 71-97.
30. Pickett B, Buell J. Usefulness of impedance cardiogram to reflect left ventricular diastolic function. Am J Cardiol, 1993; 71: 1099-1103.
31. Ramos MU. An abnormal early diastolic impedance waveform: a predictor of poor prognosis in the cardiac patients? Am Heart J, 1997; 94: 274-281.
32. Nyboer J, Bagno S, Bamet A et al. Radiocardiograms: electrical impedance changes of the heart in relation to electrocardiograms and heart sounds. J Clin Invest, 1940; 19: 963.
33. Kubicek WG, Karnegis JN, Patterson RP et al. Development and evaluation of an impedance cardiac output system. Aerosp Med, 1966; 37: 1208-1212.
34. Sramek BB. Cardiac output by electrical impedance. Med Electron, 1982; 13: 93-97.
35. Bernstein DP. A new stroke volume equation for thoracic electrical bioimpedance: theory and rationale. Crit Care Med, 1986; 14: 904-909.
36. Yakimets J, Jensen L. Evaluation of impedance cardiography: comparison of NCCOM3-R7 with Fick and thermodilution methods. Heart Lung, 1995; 24: 194-206.
37. Marik PE, Pendelton JE, Smith R. A comparison of hemodynamic parameters derived from transthoracic electrical bioimpedance with those parameters obtained by thermodilution and ventricular angiography. Crit Care Med, 1997; 25: 1545-1550.
38. De Maria AN, Raisinghani A. Comparative overview of cardiac output measurement methods: has impedance cardiography come of age? Congest Heart Fail, 2000; 6: 7-18.
39. Van De Water JM, Miller TW, Vogel RL, Mount BE, Dalton ML. Impedance cardiography. The next vital sing technology? Chest, 2003; 123: 2028-2033.
40. Strobeck JE, Silver M, Ventura
41. Sageman WS, Riffenburg RH, Spiess BD. Equivalence of bioimpedance and thermodilution in measuring cardiac index after cardiac surgery. J Cardiothorac Vasc Anesth, 2002; 16: 8-14.
42. Dranzer MH, Thompson B, Rosenberg
43. Sramek BB. Thoracic electrical bioimpedance: basic principles and physiologic relationship. Noninvas Cardiol 1994; 3: 83-8.
44. Lasater M. Managing inotrope therapy noninvasively. AACN Clin Issues 1999; 10: 406-413.
45. Weinhold C, Reichenspurner H, Fulle P, Nollert G, Reichart B. Registration of thoracic electrical bioimpedance for early diagnosis of rejection after heart transplantation. Journal of Heart and Lung Transplantation, 1993; 12: 832-836.
46. Vignon P. Hemodynamic assessment of critically ill patients using echocardiography Doppler. Curr Opin Crit Care 2005; 11: 227 – 234.
47. Axler O, Tousignant C, Thompson CR, Dallava-Santucci J et al. Comparison of transesophageal echocardiographic, fick, and thermodilution cardiac output in critically ill patients. J Crit Care 1996; 11: 109 – 116.
48. Greim CA
49. Poelaert JI, Schupfer G. Hemodynamic monitoring utilizing transesophageal echocardiography. The relations among pressure, flow and function. Chest 2005; 127: 379 – 390.
50. Bettex DA, Hinselmann V, Hellermann JP, Jenni R, Schmind ER. Transoesophageal echocardiography is unreliable for cardiac output assessment after cardiac surgery compared with thermodilution. Anaesthesia 2004; 59: 1184 – 1192.
51. Dark PM, Singer M. The validity of trans-esophageal Doppler ultrasonography as a measure of cardiac output in critically ill adults. Intensive Care Medicine 2004; 30: 2060 – 2066.
52. Darovic GO, Graham PG, Pranulis MAF. Monitoring cardiac output. In Darvic GO. Hemodynamic monitoring. Saunders 3rd edition. 2002; 245 – 262.
53. Vincent JL, De Backer D. Cardiac output measurement: Is least invasive always the best? Crit Care Med 2002; 30: 2380 – 2382.
54. Sharon Ann Hunt SA, Abraham WT, Chin MH, et al. ACC/AHA 2005 Guideline update for the diagnosis and management of chronic heart failure in the adult: a report of the American College of Cardiology / American Heart Association Task force on Practice Guidelines. Circulation 2005; 112: 154 – 235.
55. Kim RJ, Fieno DS, Parrish TB, et al. Relationship of MRI delayed contrast enhancement to irreversible injury, infarct age, and contractible function. Circulation 1999; 100: 1992 – 2002.
56. Kwong RY, Chan AK
57. Yeon SB, Sabir A, Clouse M, et al. Delayed – enhancement cardiovascular magnetic resonance coronary artery wall imaging: comparison with multislice computed tomography and quantitive coronary angiography. J Am Coll Cardiol 2007; 50: 441 – 7.
58. Oliver Gaemperli, Tiziani Schepis, Ines Valenta, et al. Cardiac image fusion from stant – alone SPECT and CT: Clinical Experience. J Nucl Med 2007; 48: 696 – 703.
59. Bax JJ, Beanlands RS, Klocke FJ, et all. Diagnostic and clinical perspectives of fusion imaging in cardiology: is the total greater than the sums of its parts? Heart 2007; 93: 16 – 22.
60. Michael C. Kontos. Myocardial perfusion imaging in the acute care setting. J Nucl Cardiology 2007; 14: 125 – 32.
61. Heinrich R. Scheibert. Focus on Molecular Imaging. J Nucl Med 2007; 48: 1915.
62. Gregory S. Thomas, MD MPH. ASNC News: A new era in Nuclear Cardiology. J Nucl Cardiology 2007; 14: 758 – 9.
63. Forssmann W. The catheterization of the right side of the heart. Klin Wockenschr. 1929; 45: 2085 – 2087.
64. Gournand A, Causon HD, Bloomfield RA, et al. Recording of right heart pressures in man. Proc Sc Exp Biol Med. 1994; 55: 34 – 36.
65. Ganz W, Donoso R, Marcus HJ, et al. A new technique for measurement of cardiac output by thermodilution in man. Am J Cardiol. 1971; 27: 392 – 396.
66. Swan HJC, Ganz W, Forrester J, et al. Catheterization of the heart in man with use of a flow directed balloon tipped catheter. N Engl J Med. 1970; 283: 447 – 451.
67. Wiener RS, Welth HG: Trends in the use of the pulmonary artery catheter in the United States, 1993 – 2004. JAMA. 2007; 298: 423 – 429.
68. Fomler RA, Cook DJ. The arc of the pulmonary artery catheter. JAMA 2003; 290: 2732 – 2734.
69. Van de Water J, Mount B
70. Mayer AF, Schroeder C, Heusser K, et al. Influences of nonepinephrine transporter function on the distribution of sympathetic activity in humans. Hypertension, 2006; 48: 120-126.
71. Piechota M, Irmanski R, Banach M, et al. Can impedance cardiography be routinely applied in patients with sepsis and severe sepsis? Archives of Medical Science. 2006, Vol: 2, issue: 2, 114 – 121.
72. Jansen JRC, Van den Berg PCM. Cardiac output by thermodilution and arterial pulse contour techniques. In Pinsky MR, Payen D (eds): Functional hemodynamic monitoring, Springer 2005; pp: 135 – 152.
73. Critchley LAH, Critchley AJH. A meta-analysis of studies using bias and precition statistics to compare cardiac output measurement techniques. J Clin Monit Comput 1999; 15: 85 – 91.
74. Nollert G, Reichart B. Registration of thoracic electrical bioimpedance for early diagnosis of rejection after heart transplantation. J Heart Lung Transplant, 1993; 12: 832 – 836.
75. Sherwood A, McFetridge J, Hutcheson JS. Ambulatory impedance cardiography: a feasibility study. J Appl Physiol, 1998; 85: 2365 – 2369.
76. Yung GL, Fedullo PF, Kinninger K, Johnson W, Channick R. Comparison of impedance cardiography to direct Fick and thermodilution cardiac output determination in pulmonary arterial hypertension. Congest Heart Fail, 2004; 10 (suppl. 2): 7 – 10.
77. Yu CM, Wang L, Chou E et al. Intrathoracic impedance monitoring in patients with heart failure: correlation with fluid status and feasibility of early warning preceding hospitalization. Circulation, 2006; 112: 841 – 848.
78. Ganion V, Rhodes M, Stadler RW. Intrathoracic impedance to monitor heart failure status: a comparison of two methods in chronic heart failure dog model. Congest Heart Fail, 2005; 211: 177 – 181.
79. Forrester JS, Diamond G, Chatterjee K, Swan HJC. Correlative classification of clinical and hemodynamic function after acute myocardial infarction. J Am Cardiol 1997; 39: 137 – 145.
80. Nawarycz T, Ostrowska - Nawarycz L, Kaczmarek J. Impact of cardiovascular reaction using the impedance cardiography method in borderline hypertension. Ann Acad Sci, 1999; 873: 174 – 181.
81. Verhoeve PE Cadwell CA
82. Heerdt PM, Pond CG, Blessios GA
83. Botero M, Kirby D, Lobato EB, Staples ED, Gravenstein N. Measurement of cardiac output before and after cardiopulmonary bypass: Comparison among aortic transit – time ultrasound, thermodilution, and noninvasive partial CO2 rebreathing. J Cardiothorac Vasc Anesth, 2004; 18: 562 – 564.
84. Myles PS, Gin T. Statistical methods for anesthesia and intensive care. Elsevier 2000; 90 – 92.
85. Bajorat J, Hofmockel R, Vagts DA, Janda M, Pohl B, Beck C, Noeldge-Schmburg G. Comparison of invasive and less – invasive techniques of cardiac output measurement under different haemodynamic conditions in a pig model. Eur J Anesthesiol 2006; 23: 23 – 30.
86. Hogue CW, Rosenbloom M, McCawley C, Lappas DG. Comparison of cardiac output measurement by continuous thermodilution with electromagnetometry in adult cardiac surgical patients. J Cardiothorac Vasc Anesth. 1994; 8: 631 – 635.
87. Ganz W, Swan HJ. Measurement of blood flow by thermodilution. Am J Cardiol. 1972; 29: 241 – 246.
88. Nilsson LB, Nilsson JC, Skovgaard LT, Berthelsen PG. Thermodilution cardiac output - are three injections enough? Acta Anaesthesiol Scand. 2004; 48: 1322 – 1327.
89. Fuller HD. The validity of cardiac output measurement by thoracic impedance: a meta – analysis. Clin Invest Med 1992; 15: 103 – 12.
90. Raaijmakers E, Faes TJ, Scholten J, Goovaerts G, Heethaar RM. A meta – analysis of three decades of validating thoracic impedance cardiography. Crit Care Med 1999; 27: 1203 – 13.
91. Shoemaker WC, Belzberg H, Wo CJ, Miltzman DP, et al. Multicenter study of noninvasive monitoring systems as alternatives to invasive monitoring of acutely ill emergency patients. CHEST 1998; 114: 1643 – 1652.
92. Edmunds AT, Godfrey S, Tooley M. Cardiac output measurement by transthoracic impedance cardiography at rest, during exercise and at various lung volumes. Clin Sci 1982; 63(2): 107 – 13.
93. Summers R, Schoemaker W, Peacock WF, Ander D, Coleman T. Bench to bedside series: Impedance cardiography (ICG). Acad Emerg Med 2003; 10(6): 669 – 680.
94. Voulgari C, Tendolouris N, Moussakis I, Dilaveris P, Gialafos E, Papadogiannis D, et al. The spatial QRS-T angle: association with diabetes and left ventricular performance. Eur J Clin Invest 2006; 36: 608 – 613.
95. Bergstrom B, Manhem P, Bramnert M, Lilja B, Sundkvist G. Impaired responses of plasma catecholamines to exercise in diabetic patients with abnormal heart rate reactions to tilt. Clin Physiol 1989; 9: 259 – 267.
96. Batchvarov V, Dilaveris P, Farbom P, Ghuran A, Acar B, Hnatkova K, et al. New description of homogeneity of the propagation of ventricular repolarization. Pacing Clin Electrophysiol 2000, 23: 1968 – 1972.
Galt J, Garsia E, Robbins W. Effects of myocardial wall thickness on SPECT quantification. IEEE Trans Med Imag 